 Spektrofotometer adalah alat untuk
mengukur transmitan atau absorban suatu sampel sebagai fungsi panjang
gelombang. Spektrofotometer merupakan gabungan dari alat optik dan elektronika
serta sifat-sifat kimia fisiknya dimana detektor yang digunakan secara langsung
dapat mengukur intensitas dari cahaya yang dipancarkan (It) dan secara tidak
lansung cahaya yang diabsorbsi (Ia), jadi tergantung pada spektrum
elektromagnetik yang diabsorb (serap) oleh benda. Tiap media akan menyerap
cahaya pada panjang gelombang tertentu tergantung pada senyawaan atau warna
terbentuk.
Spektrofotometer adalah alat untuk
mengukur transmitan atau absorban suatu sampel sebagai fungsi panjang
gelombang. Spektrofotometer merupakan gabungan dari alat optik dan elektronika
serta sifat-sifat kimia fisiknya dimana detektor yang digunakan secara langsung
dapat mengukur intensitas dari cahaya yang dipancarkan (It) dan secara tidak
lansung cahaya yang diabsorbsi (Ia), jadi tergantung pada spektrum
elektromagnetik yang diabsorb (serap) oleh benda. Tiap media akan menyerap
cahaya pada panjang gelombang tertentu tergantung pada senyawaan atau warna
terbentuk.
Yang perlu dikalibrasi adalah
panjang gelombang dan absorbansi
Kalibrasi Panjang gelombang
- menggunakan filter gelas holium oksida yang memupnyai panjang gelombang acuan (nm)
- pasang filter gelas holium oksida pada kompartemen sampel dan kompartemen pembanding dibiarkan kosong (udara)
- Scan spektrum serapan holium oksida, bandingkan panjang gelombang spektrum yang diperoleh dengan data panjang gelombang acuan.
Kalibrasi Absorbans
Buat larutan kalium dikromat 100 + 1 mg dalam 1 liter 0,005 mol/L asam sulfat (larutan B)
buat larutan 0,005 mol/L asam sulfat sebagai pembanding dan bandingkan hasilnya dengan data acuan (+ 2%)
PRINSIP
Spektrofotometri serapan atom (AAS) adalah suatu metode analisis yang didasarkan pada proses penyerapan energi radiasi oleh atom-atom yang berada pada tingkat energi dasar (ground state). Penyerapan tersebut menyebabkan tereksitasinya elektron dalam kulit atom ke tingkat energi yang lebih tinggi. Keadaan ini bersifat labil, elektron akan kembali ke tingkat energi dasar sambil mengeluarkan energi yang berbentuk radiasi.
Dalam AAS, atom bebas berinteraksi dengan berbagai bentuk energi seperti energi panas, energi elektromagnetik, energi kimia dan energi listrik. Interaksi ini menimbulkan proses-proses dalam atom bebas yang menghasilkan absorpsi dan emisi (pancaran) radiasi dan panas.
Spektrofotometri serapan atom (AAS) adalah suatu metode analisis yang didasarkan pada proses penyerapan energi radiasi oleh atom-atom yang berada pada tingkat energi dasar (ground state). Penyerapan tersebut menyebabkan tereksitasinya elektron dalam kulit atom ke tingkat energi yang lebih tinggi. Keadaan ini bersifat labil, elektron akan kembali ke tingkat energi dasar sambil mengeluarkan energi yang berbentuk radiasi.
Dalam AAS, atom bebas berinteraksi dengan berbagai bentuk energi seperti energi panas, energi elektromagnetik, energi kimia dan energi listrik. Interaksi ini menimbulkan proses-proses dalam atom bebas yang menghasilkan absorpsi dan emisi (pancaran) radiasi dan panas.
Radiasi yang dipancarkan bersifat khas karena mempunyai panjang gelombang yang karakteristik untuk setiap atom bebas.
Adanya absorpsi atau emisi radiasi disebabkan adanya transisi elektronik yaitu perpindahan elektron dalam atom, dari tingkat energi yang satu ke tingkat energi yang lain.
Absorpsi radiasi terjadi apabila ada elektron yang mengabsorpsi energi radiasi sehingga berpindah ke tingkat energi yang lebih tinggi.
Emisi terjadi apabila ada elektron yang berpindah ke tingkat energi yang lebih rendah sehingga terjadi pelepasan energi dalam bentuk radiasi.
Panjang gelombang dari radiasi yang menyebabkan eksitasi ke tingkat eksitasi tingkat-1 disebut panjang gelombang radiasi resonansi. Radiasi ini berasal dari unsur logam/metaloid.
Radiasi resonansi dari unsur X hanya dapat diabsorpsi oleh atom X, sebaliknya atom X tidak dapat mengabsorpsi radiasi resonansi unsur Y. Tak ada satupun unsur dalam susunan berkala yang radiasi resonansinya menyamai unsur lain.
Hal inilah yang menyebabkan metode AAS sangat spesifik dan hampir bebas gangguan karena frekuensi radiasi yang diserap adalah karakteristik untuk setiap unsur. Gangguan hanya akan terjadi apabila panjang radiasi resonansi dari dua unsur yang sangat berdekatan satu sama lain.
Sekitar 67 unsur telah dapat ditentukan dengan cara AAS. Banyak penentuan unsur-unsur logam yang sebelumnya dilakukan dengan metoda polarografi, kemudian dengan metoda spektrofotometri UV-VIS, sekarang banyak diganti dengan metoda AAS.
Keuntungan metoda AAS adalah:
•Spesifik
•Batas (limit) deteksi rendah
•Dari satu larutan yang sama, beberapa unsur berlainan dapat diukur
•Pengukuran dapat langsung dilakukan terhadap larutan contoh (preparasi contoh sebelum pengukuran lebih sederhana, kecuali bila ada zat pengganggu)
•Dapat diaplikasikan kepada banyak jenis unsur dalam banyak jenis contoh.
•Batas kadar-kadar yang dapat ditentukan adalah amat luas (mg/L hingga persen)
Atomisasi
Ada tiga cara atomisasi (pembentukan atom) dalam AAS :
1.Atomisasi dengan nyala
Suatu senyawa logam yang dipanaskan akan membentuk atom logam pada suhu ± 1700 ºC atau lebih. Sampel yang berbentuk cairan akan dilakukan atomisasi dengan cara memasukan cairan tersebut ke dalam nyala campuran gas bakar. Tingginya suhu nyala yang diperlukan untuk atomisasi setiap unsur berbeda.
Beberapa unsur dapat ditentukan dengan nyala dari campuran gas yang berbeda tetapi penggunaan bahan bakar dan oksidan yang berbeda akan memberikan sensitivitas yang berbeda pula.
Syarat-syarat gas yang dapat digunakan dalam atomisasi dengan nyala:
•Campuran gas memberikan suhu nyala yang sesuai untuk atomisasi unsur yang akan dianalisa
•Tidak berbahaya misalnya tidak mudah menimbulkan ledakan.
•Gas cukup aman, tidak beracun dan mudah dikendalikan
•Gas cukup murni dan bersih (UHP)
Campuran gas yang paling umum digunakan adalah Udara : C2H2 (suhu nyala 1900 – 2000 ºC), N2O : C2H2 (suhu nyala 2700 – 3000 ºC), Udara : propana (suhu nyala 1700 – 1900 ºC)
Banyaknya atom dalam nyala tergantung pada suhu nyala. Suhu nyala tergantung perbandingan gas bahan bakar dan oksidan.
Hal-hal yang harus diperhatikan pada atomisasi dengan nyala :
1.Standar dan sampel harus dipersiapkan dalam bentuk larutan dan cukup stabil. Dianjurkan dalam larutan dengan keasaman yang rendah untuk mencegah korosi.
2.Atomisasi dilakukan dengan nyala dari campuran gas yang sesuai dengan unsur yang dianalisa.
3.Persyaratan bila menggunakan pelarut organik :
•Tidak mudah meledak bila kena panas
•Mempunyai berat jenis > 0,7 g/mL
•Mempunyai titik didih > 100 ºC
•Mempunyai titik nyala yang tinggi
•Tidak menggunakan pelarut hidrokarbon
Pembuatan atom bebas dengan menggunakan nyala (Flame AAS)
Contoh: Suatu larutan MX, setelah dinebulisasi ke dalam spray chamber sehingga terbentuk aerosol kemudian dibawa ke dalam nyala oleh campuran gas oksidan dan bahan bakar akan mengalami proses atomisasi
2.Atomisasi tanpa nyala
Atomisasi tanpa nyala dilakukan dengan mengalirkan energi listrik pada batang karbon (CRA – Carbon Rod Atomizer) atau tabung karbon (GTA – Graphite Tube Atomizer) yang mempunyai 2 elektroda.
Sampel dimasukan ke dalam CRA atau GTA. Arus listrik dialirkan sehingga batang atau tabung menjadi panas (suhu naik menjadi tinggi) dan unsur yang dianalisa akan teratomisasi. Suhu dapat diatur hingga 3000 ºC. pemanasan larutan sampel melalui tiga tahapan yaitu :
•Tahap pengeringan (drying) untuk menguapkan pelarut
•Pengabuan (ashing), suhu furnace dinaikkan bertahap sampai terjadi dekomposisi dan penguapan senyawa organik yang ada dalam sampel sehingga diperoleh garam atau oksida logam
•Pengatoman (atomization)
3.Atomisasi dengan pembentukan senyawa hidrida
Atomisasi dengan pembentukan senyawa hidrida dilakukan untuk unsur As, Se, Sb yang mudah terurai apabila dipanaskan pada suhu lebih dari 800 ºC sehingga atomisasi dilakukan dengan membentuk senyawa hibrida berbentuk gas atau yang lebih terurai menjadi atom-atomnya melalui reaksi reduksi oleh SnCl2 atau NaBH4, contohnya merkuri (Hg).
Skema peralatan AAS
1.Sumber radiasi berupa lampu katoda berongga
2.Atomizer yang terdiri dari pengabut dan pembakar
3.Monokromator
4.Detektor
5.Rekorder
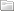 Label:
Label:
 Rabu, 28 November 2012
Rabu, 28 November 2012





