anggota kelompok
1. Rela Religia Amalia
2. Rima Sundari
3. Ririn Puji Astuti
4. Risti Intan Prastiwi
DEFINISI
Elektroda Selektif Ion (ESI) merupakan metoda yang digunakan untuk menentukan konsentrasi suatu ion secara kuantitatif dengan menggunakan membran sebagai sensor kimia yang potensialnya berubah secara reversibel terhadap perubahan aktivitas ion yang ditentukan. Membran merupakan bagian terpenting yang menentukan selektivitas suatu ESI. Penelitian ini bertujuan untuk membuat ESI iodida menggunakan campuran AgI, grafit, dan parafin cair dengan tiga komposisi yang berbeda, mempelajari pengaruh variasi perbandingan relatif komponen elektroda terhadap selektivitas membran, dan mempelajari karakter ESI iodida yang meliputi nilai faktor Nernst, koefisien selektivitas potensiometri, dan limit deteksi.
PENENTUAN KADAR ION SIANIDA
1. Rela Religia Amalia
2. Rima Sundari
3. Ririn Puji Astuti
4. Risti Intan Prastiwi
DEFINISI
Elektroda Selektif Ion (ESI) merupakan metoda yang digunakan untuk menentukan konsentrasi suatu ion secara kuantitatif dengan menggunakan membran sebagai sensor kimia yang potensialnya berubah secara reversibel terhadap perubahan aktivitas ion yang ditentukan. Membran merupakan bagian terpenting yang menentukan selektivitas suatu ESI. Penelitian ini bertujuan untuk membuat ESI iodida menggunakan campuran AgI, grafit, dan parafin cair dengan tiga komposisi yang berbeda, mempelajari pengaruh variasi perbandingan relatif komponen elektroda terhadap selektivitas membran, dan mempelajari karakter ESI iodida yang meliputi nilai faktor Nernst, koefisien selektivitas potensiometri, dan limit deteksi.
PENENTUAN KADAR ION SIANIDA
TUJUAN:
Untuk mengetahui dan
mempelajari penerapan Potensiometris penentuan ion tertentu dan juga menetukan
kadar ion Sianida menggunakan Elektroda Ion Selektif.
PRINSIP:
Metoda Potensiometri
merupakan suatu cara analisa yang didasarkan pada pengukuran beda potensial yang terjadi diantara
sepasang elektroda yaitu elektroda pembanding dan elektroda
indikator
Elektroda ion
selektif yang kita gunakan dalam praktikum kali ini merupakan elektroda indikator, dimana harga potensial terukur
dipengaruhi oleh aktivitas ion atau konsentrasi larutan.Pada
praktikum menggunakan larutan sianida dengan konsentrasi 1000 ppm
CARA KERJA :
1.Siapkan 6 buah labu ukur
50 ml
2.Labu kedua
masukkan ujung buret, masukkan 50 ml
3.Tekan dengan
hati-hati tombol go untuk mengeluarkan 0,050 ml larutan standar 1000 ppm CN-
4.Cara yang sama dengan
yang di atas
5.Keluarkan 0,200 ;
0,800 ; 3,200 ; 12,800 ml larutan standar CN- 1000 ppm ke dalam labu ke 3 s/d ke 6 (jadi labu 1 tidak berisi standar CN-)
6.Tambahkan 5 ml NaOH 1 N
lalu encerkan sampai batas dengan akuades maka akan
didapatkan deretan standar 0 , 1 , 4 , 16 , 64 , 256 ppm CN-)
7.Pasangkan elektroda
kombinasi ion selektif CN- pada alat pH/ion meter Celupkan elektroda beserta thermometer
kepada larutan blanko
8.Ukur suhunya dan
atur tombol koreksi suhu pada nilai suhu larutan dengan menekan tombol
up/down
9.Tekan mode untuk memilih
fungsi Mv
10. Biarkan stabil dan
catat nilai beda potensial yang ditunjukkan sebagai E dalam MV
11.Keluarkan blanko ganti dengan
deretan standar 1 ppm tunggu stabil, catat nilai E-nya.
12.Lakukan hal yang sama
terhadap standar lainnya (2-6)
13.Masukkan sampel ke dalam
labu ukur 50 ml
14.Tambahkan 5 ml NaOH 1 N,
encerkan sampai batas dengan akuades
15.Pindahkan deretan
standar ini pada gelas piala
16.Celupkan elektroda
beserta thermometer pada larutan sampel
17.Perlakukan hal yang
sama seperti perlakuan standar
18.Catat Nilai potensial
yang dihasilkan
19.Buatlah kurva
kalibrasi standar antara yaitu :
E vs –log C pada kertas grafik biasa
E vs C pada kertas grafik semi blog
20.Tentukan kadar ion Sianida
(CN-) dari larutan sampel.
Skema Elektroda Selektif Ion
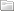 Label:
Label:
 Rabu, 07 November 2012
Rabu, 07 November 2012




